作者简介:张倩(1982-),女,博士研究生,从事黏合剂用高分子的设计、合成和性能研究。E-mail:qian3545267@163.com 通信作者:刘宁(1984-),男,研究员,从事含能材料的设计、合成及性能研究。E-mail:flackliu@sina.com
(西安近代化学研究所,陕西 西安 710065)
(Xi'an Modern Chemistry Research Institute, Xi'an 710065, China)
organic chemistry; azide terminated; urethane; hydroxyl terminated ethylene oxide tetrahydrofuran copolyether; PET; 2-chloroethyliso cyanate
DOI: 10.14077/j.issn.1007-7812.201907006.
备注
作者简介:张倩(1982-),女,博士研究生,从事黏合剂用高分子的设计、合成和性能研究。E-mail:qian3545267@163.com 通信作者:刘宁(1984-),男,研究员,从事含能材料的设计、合成及性能研究。E-mail:flackliu@sina.com
为了解决端羟基环氧乙烷-四氢呋喃无规共聚醚黏合剂的固化过程水敏感问题,以端羟基环氧乙烷-四氢呋喃无规共聚醚(PET)为母体聚合物,首先与2-氯乙基异氰酸酯经过亲核加成反应制备出一种含氨基甲酸酯基团的端氯基共聚醚中间体(ClTUPET),再通过与叠氮化钠的亲核取代反应制备得到了含有氨基甲酸酯结构单元的端叠氮基四氢呋喃-环氧乙烷无规共聚醚(ATUPET),探讨了ATUPET的合成机理; 采用红外光谱、核磁共振碳谱、凝胶渗透色谱、DSC以及TGA对产物的结构和性能进行了表征。结果 表明,端位羟基转化完全,成功制备出了ATUPET,该合成方法简单,收率93.98%; ATUPET的玻璃化转变温度-69.4℃,冷结晶温度-47.2℃,熔点约为-8.6℃,热分解温度大于200℃,具有良好的热稳定性。
The azide terminated ethylene oxide-tetrahydrofuran copolyether with urethane segments(ATUPET)was designed to solve its sensitivity to humidity during the curing process. It was prepared by a two-step method. Firstly, chloro terminated ethylene oxide-tetrahydrofuran copolyether with urethane segments(ClTUPET)was synthesized by nucleophilic addition between hydroxyl terminated ethylene oxide-tetrahydrofuran copolyether(PET)and 2-chloroethyl isocyanate. Then ATUPET was synthesized by nucleophilic substitution of ClTUPET with sodium azide. The product was characterized by IR, 13C NMR, GPC, and DSC. The results indicate that the hydroxyl group disappears after modification with high yield of 93.98%. Meanwhile, the glass transition temperature of ATUPET is -69.4℃. Its cold crystallization temperature and melting temperature are -47.2℃ and -8.6℃, respectively. The thermal decomposition temperature of ATUPET is more than 200℃, showing that ATUPET has a satisfactory thermal stability.
引言
在固体推进剂领域,端羟基聚醚类黏合剂预聚物不仅自身具有良好的物理化学性质,并且和硝酸酯类增塑剂具有较好的相容性,因此其在NEPE推进剂中有着重要而广泛的应用[1-2]。但是,端羟基聚醚预聚物在应用过程中,需要和异氰酸酯类固化剂反应形成聚氨酯弹性体[3]。然而,聚氨酯类弹性体的制备和使用过程中仍存在一定的问题:一方面,固化剂原料中含有活泼的异氰酸酯基,其极易与水反应形成脲,并释放出二氧化碳气体,造成推进剂在加工过程中会有气泡产生从而影响其正常使用[4]; 另一方面,聚氨酯弹性体与高能氧化剂组分(如ADN、HNF)的相容性差,进而限制了其在高能配方中的应用[5-7]。因此,非异氰酸酯固化技术一直是该领域的研究热点之一。
2001年,丹麦的Medal[8]和美国的Sharpless[9]分别独立发现了铜催化的端炔基和叠氮化合物的Huisgen 1,3-偶极环加成反应,简称CuAAC反应(Cu-catalyzed azide-alkyne 1,3-dipolar cycloaddition)。CuAAC反应作为“点击化学”中的最具代表性的反应,已在生物医学、材料化学等领域得到了广泛的应用和研究[10-12]。同时,由于该反应条件温和,对水分不敏感、无副产物,与一些高能氧化剂组分具有较好的相容性等诸多优点,使其在推进剂领域中具有广阔的应用前景。目前,有诸多改性黏合剂基于CuAAC反应原理进行固化的文献报道[13-16]。在对于端羟基聚醚的改性研究中,主要通过端叠氮化改性[17]或者端炔基化[18]改性两种方式进行。其中,北京理工大学的翟进贤等[19]采用端羟基环氧乙烷-四氢呋喃无规共聚醚(PET)经氯化-叠氮化两步反应制备得到端叠氮基PET(APET),并利用三炔丙基胺对其进行固化,所得到的聚三唑弹性体抗张强度为1.45MPa,模量为2.22MPa,断裂延伸率为125%,具有良好的力学性能。然而,基于APET的聚三唑结构,由于缺少氨酯键的引入,其内聚能密度相对较低,力学性能仍有进一步提高的空间。
本研究为进一步提高聚三唑弹性体的力学性能,首次合成出了一种含有氨基甲酸酯基团的端叠氮基环氧乙烷-四氢呋喃无规共聚醚(简称ATUPET)。在该聚合物的结构设计中,叠氮基团和氨基甲酸酯基团均位于共聚醚分子链的两端:一方面,叠氮基团属于参与固化反应的官能团,其可以与炔键发生固化反应从而实现预聚物的非异氰酸酯固化; 另一方面,氨基甲酸酯基团具有较强的氢键作用,有利于聚三唑弹性体网络结构中硬链段的聚集,促进弹性体的微相分离,可以在一定程度上促进聚三唑弹性体的力学性能的进一步提高。
1 实 验
1.1 试剂与仪器环氧乙烷-四氢呋喃无规共聚醚(PET),黎明化工研究院; 2-氯乙基异氰酸酯,化学纯,百灵威科技有限公司; 二月桂酸二丁基锡(DBTDL)、叠氮化钠、N,N-二甲基甲酰胺和二氯甲烷,均为化学纯,成都科龙化工试剂厂。
AV500型超导核磁共振波谱仪、TENSOR27型傅里叶变换红外光谱仪,德国Bruker公司; CAP2000+型黏度计,美国Brookfield公司; DCS200 F3型差示扫描量热仪、STA 449热重分析仪,德国Netzsch公司。
1.2 端氯基环氧乙烷-四氢呋喃无规共聚醚(ClTUPET)的合成向配有机械搅拌,冷凝管和温度计的三口圆底烧瓶中加入PET(21.29g,5mmol)、2-氯乙基异氰酸酯(2.11g,20mmol)以及一定量的催化剂DBTDL,搅拌均匀后缓慢升温至90℃,反应18h。反应结束后除去过量的2-氯乙基异氰酸酯,得到无色黏稠液体为端氯基环氧乙烷-四氢呋喃无规共聚醚,质量22.31g,收率99.83%。
1.3 端叠氮基环氧乙烷-四氢呋喃无规共聚醚(ATUPET)的合成向配有机械搅拌、回流冷凝管,温度计的250mL三口圆底烧瓶中依次加入ClTUPET(20.11g,4.5mmol)、50mL N,N-二甲基甲酰胺以及叠氮化钠(1.76g,27mmol),搅拌均匀后缓慢升温至90℃,反应48h。反应结束后,减压蒸除溶剂,得到橙黄色黏稠状液体即为端叠氮基环氧乙烷-四氢呋喃嵌段共聚醚,质量19.85g,收率93.98%。
2 结果与讨论
3 结 论
(1)通过亲核加成和亲核取代两步法合成得到了含有氨基甲酸酯结构的端叠氮基四氢呋喃-环氧乙烷无规共聚醚黏合剂。此法具有合成简单、容易操作且收率较高的特点。
(2)通过FT-IR,13C NMR及GPC的谱图分析,证明了所得产物为目标聚合物ATUPET,并且确认端基转化完全。
(3)ATUPET的玻璃化转变温度为-69.4℃,保证了推进剂良好的低温性能; 其冷结晶温度为-47.2℃,熔点约为-8.6℃,在常温状态下为液体,能够更好地作为推进剂黏合剂使用,具有较好的工艺性能; ATUPET的热分解峰温大于200℃,具有良好的热稳定性。
2.1 ATUPET的合成机理ATUPET的合成过程由两步反应实现:首先,PET预聚物中的端位羟基与2-氯乙基异氰酸酯发生亲核加成反应,生成含有氨基甲酸酯结构单元的端氯基ClTUPET中间体; 其次,由于Cl原子的电负性大于碳原子,是很好的离去基团,容易在非质子偶极溶剂中被取代,因此在DMF中,ClTUPET端位的-Cl作为易于离去基团,被-N3所取代,从而得到端叠氮基ATUPET。其具体的反应历程如下所示:
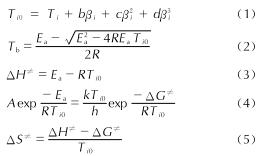
由上述反应机理可以看出,在第一步PET与2-氯乙基异氰酸酯的亲核加成反应中,由于此反应对水敏感,因此反应前需要对原料PET进行除水操作; 同时,为了提高反应速率,本合成方法采用本体法进行,同时加入二丁锡基二月桂酸酯作为反应催化剂。在具体实验过程中,对PET和2-氯乙基异氰酸酯的投料摩尔比为1:2、1:4和1:6进行了研究。理论上,投料摩尔比1:2反应即可实现,但在实际反应过程中,产物的核磁分析则显示仍有极少部分羟基没有发生反应,这可能是由于羟值的测定和实际值之间存在一定的误差,同时,反应过程中,不可避免的极少量水份对于原料异氰酸酯的损耗以及2-氯异氰酸酯在反应过程中会少量气化后与反应瓶上方位置液化成液滴,从而使得端基无法转化完全。而1:6的投料摩尔比,则会增加后处理的难度和时间。因此,综合考量选择PET和2-氯乙基异氰酸酯的摩尔比为1:4作为反应最优投料比。
2.2 ATUPET的结构表征2.2.1 红外光谱图分析PET和ATUPET的红外光谱图如图1所示。
由图1可知,在PET的红外光谱图中,3484cm-1处的宽峰为端位羟基(—OH)的振动吸收峰,2939、2861和1356cm-1为C—H的对称、不对称以及变形振动吸收峰,而1115cm-1的特征强峰则为典型的醚键(—C—O—C—)的吸收峰。同时,在ATUPET的红外光谱中可以看到,端位改性后的聚合物其聚醚链段基本的骨架结构没有发生改变,原PET的羟基(—OH)特征宽峰已经消失,而相对应的在3510cm-1和3330cm-1两处则出现了氨基甲酸酯结构单元中的—NH的伸缩振动特征峰,在1725cm-1附近的强的吸收峰则为氨基甲酸酯结构单元中—C=O的吸收峰。此外,2100cm-1处为典型的—CH2—N3的振动吸收。
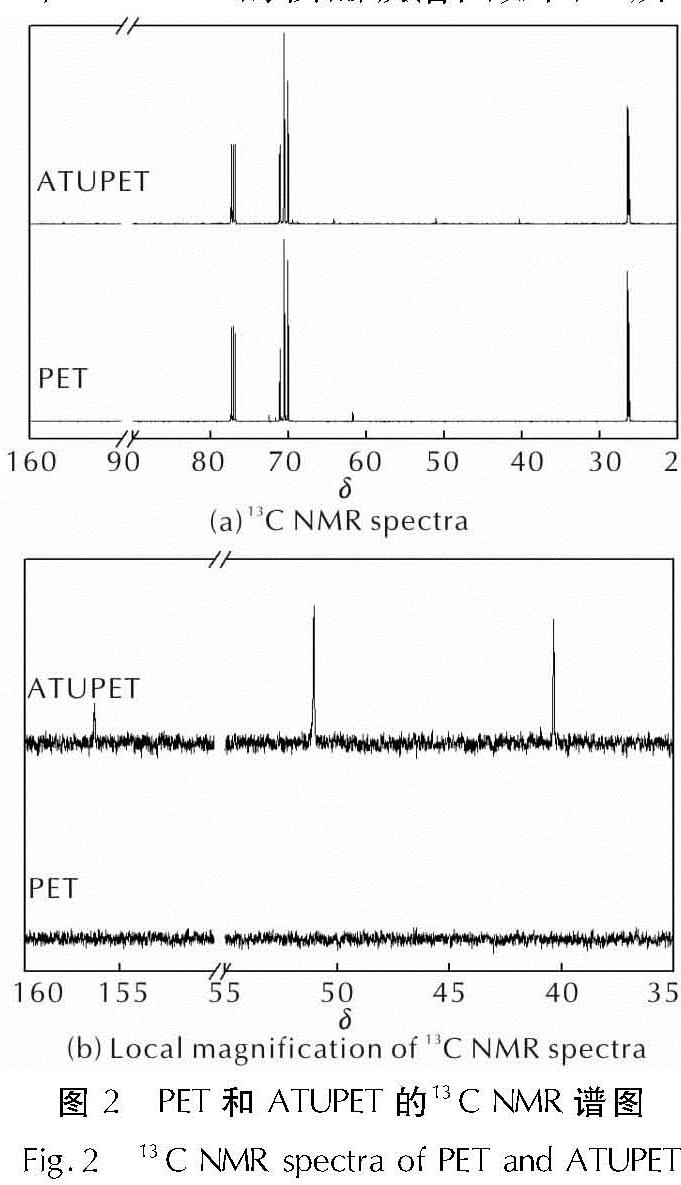
2.2.2 13C NMR核磁共振谱图分析PET和ATUPET的核磁碳谱图如图2所示。
图2 PET和ATUPET的13C NMR谱图
Fig.2 13C NMR spectra of PET and ATUPET由图2可知,在PET的13C NMR谱图中可以看到,其四氢呋喃及聚乙二醇链段中与氧相连的碳原子(—OCH2CH2O—和—OCH2CH2CH2CH2O—)化学位移在70左右的多重峰,而四氢呋喃链段中不与氧连接的碳原子(—OCH2CH2CH2CH2O—)化学位移在26左右,而与末端羟基相连的碳原子的化学位移在61.75和61.68左右。对于改性的聚合物ATUPET的13C NMR谱图可以看出,其分子链骨架没有发生变化,同时,由于氨基甲酸酯结构的生成,原来与末端羟基相连的碳原子的信号峰消失,说明端位羟基与2-氯乙基异氰酸酯反应完全,而在64.28和64.19出现两个新峰对应于与氨基甲酸酯结构单元相连接的两种碳原子(—CH2OCONH—),而—C=O的化学位移则出现在156.35,此外,分子链末端与—N3相连的α-C(—OCONHCH2CH2N3),β-C(—OCONHCH2CH2N3)的化学位移则分别出现在43.88和42.79附近。
2.3 凝胶色谱分析采用GPC对原料及产物ATUPET的相对分子量及其分布进行了分析,其结果见表1。
由表1可以看出,相对于母体聚合物PET,改性聚合物ATUPET的数均分子量略有上升,相对分子质量分布未发生较大变化,说明本反应合成的目标聚合物未发生分子链断裂或者延链等副反应。
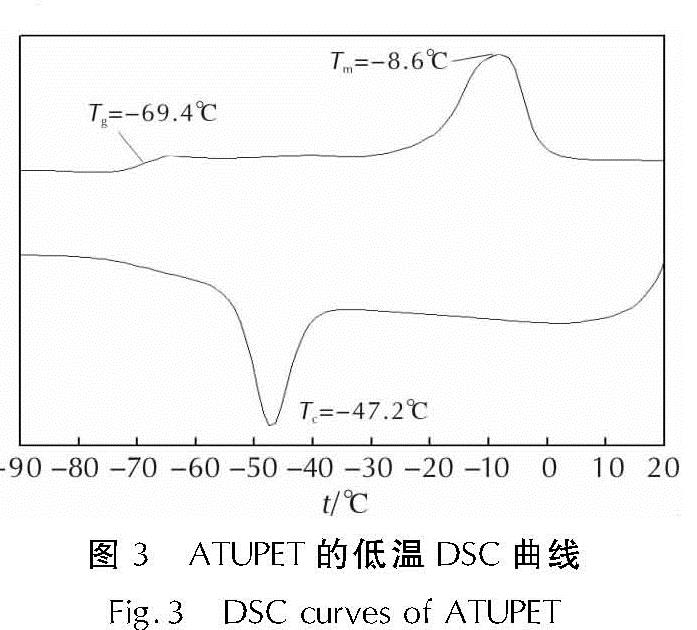
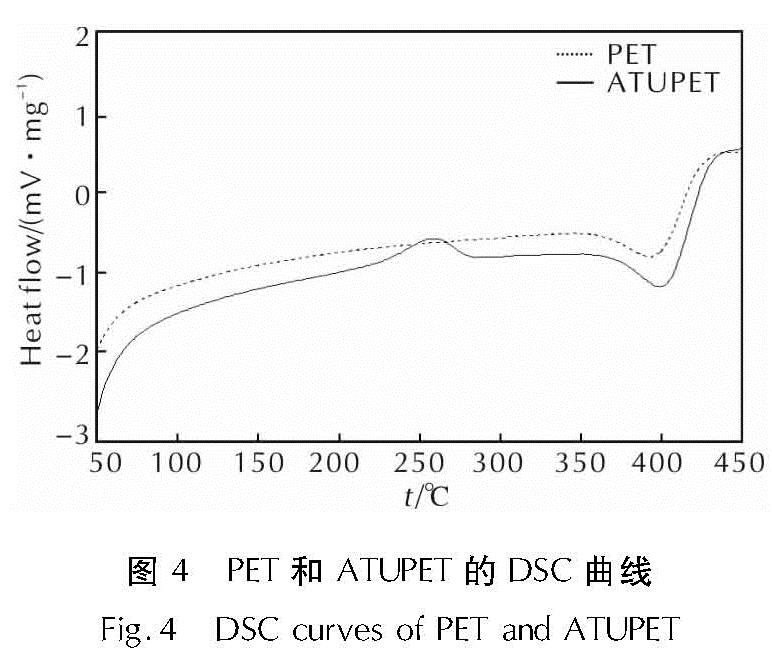
2.4 玻璃化转变温度本研究采用DSC法测定了ATUPET的玻璃化转变温度(Tg)为-69.4℃,而原料PET的玻璃化转变温度为-71.3℃。由此可见,通过向PET分子链的两端引入含有氨基甲酸酯结构单元的端叠氮基团,由于氨基甲酸酯结构单元具有较强的氢键作用,使得ATUPET的共聚醚链段的自由运动受到进一步限制,即主链柔顺性变差,进而使得改性后的ATUPET的Tg相对于母体PET有所升高。但是,相对于GAP等玻璃化转变温度较高的含能黏合剂来说,ATUPET的玻璃化转变温度仍然较低,可以保证弹性体的低温力学性能,满足推进剂的低温使用要求。此外,从低温DSC谱图(见图3)还可以看出,ATUPET的冷结晶温度为-47.2℃,ATUPET的熔点约为-8.6℃,因此其在常温状态下为液体,能够更好地作为推进剂黏合剂使用。
- [1] 任治,李笑江,王晗,等. 硝化棉/端羟基聚醚共混物的制备及其相容性研究[J]. 中国胶黏剂, 2015, 24(3):6-9.
- [2]周水平, 吴芳, 唐根, 等. CL-20含量及其粒度级配对NEPE推进剂燃烧性能的影响[J]. 火炸药学报, 2020,42(2):195-202.
- [3]张铂. HTPE端羟基聚醚的合成与表征及其与异氰酸酯反应的研究[D]. 洛阳:河南科技大学,2017.
- [4]LI Na,ZHAO Feng-qi,LUO Yang,et al. Study on curing reaction thermokinetics of azide binder/bispropargyl succinate by microcalorimetry [J]. Propellants, Explosives, Pyrotechnics, 2015,40: 808-813
- [5]MENKE K, HEINTZ T, SCHWEIKERT W,et al. Formulation and properties of ADN/GAP propellants [J]. Propellants, Explosives, Pyrotechnics,2009,34(3):218-230.
- [6]KEICHER T, KUGLSTATTER W, EISELE S,et al. Isocyanate-free curing of glycidyl azide polymer(GAP)with bis-propargyl-succinate(II)[J]. Propellants, Explosives, Pyrotechnics, 2009,34(3):210-217.
- [7]LEE D H, KIM K T, JANG Y, et al. 1,2,3-Triazole crosslinked polymers as binders for solid rocket propellants [J]. Journal of Applied Polymer Science,2014,131(15):40594.
- [8]TORNØE C W, C, MEDAL M. Peptidotriazoles on solid phase: [1,2,3]-triazoles by regiospecific copper(I)-catalyzes 1,3-dipolar cycloadditions of terminal alkynes to azides [J]. The Journal of Organic Chemistry, 2002, 67: 3057-3064.
- [9]ROSTOVTSEV V V, GREEN L G, FOKIN V V, et al. A stepwise huisgen cycloaddition process: copper(I)-catalyzed regioselective “ligation” of azides and terminal alkynes[J]. Angewandte Chemie International Edition, 2002, 41(14): 2596-2599.
- [10]HUISGEN R. Kinetics and mechanism of 1,3-dipolar cycloadditions [J]. Angewandte Chemie International Edition in English,1963,2(11):633-645.
- [11]FIRESTONE R A. Mechanism of 1,3-dipolar cycloadditions [J]. The Journal of Organic Chemistry,1968,33(6):2285-2290.
- [12]BINAULD S, DAMIRON D, HAMAIDE T, et al. Click chemistry step growth polymerization of novel alpha-azide-omega-alkyne monomers [J]. Chemical Communications,2008,35:4138-4140.
- [13]LI H, YU Q, ZHAO F, et al. Polytriazoles based on alkyne terminated polybutadiene with and without urethane segments: morphology and properties [J]. Journal of Applied Polymer Science, 2017,134(32):45178.
- [14]DING Y, HU C, GUO X, et al. Structure and mechanical properties of novel composites based on glycidyl azide polymer and propargyl-terminated polybutadiene as potential binder of solid propellant [J]. Journal of Applied Polymer Science,2013,131(7):40007
- [15]RESHMI S, VIJALAKSHMI K P, THOMAS D, et al. Polybutadiene crosslinked by 1,3-dipolar cycloaddition: pyrolysis mechanism, DFT studies and propellant burning rate characteristics [J]. Combustion and Flame,2016,167:380-391.
- [16]LEE D H, KIM K T, JUNG H, et al. Characterization of 1,2,3-triazole crosslinked polymers based on azide chain-ends prepolymers and a dipolarophile curing agent as propellant binders: The effect of a plasticizer [J]. Journal of the Taiwan Institute of Chemical Engineers,2014,45(6):3110-3116.
- [17]RESHMI S, HEMANTH H, GAYATHRI S, et al. Polyether triazoles: an effective binder for ‘green' gas generator solid propellants [J]. Polymer,2016,92:201-209.
- [18]QU Z, ZHAI J, YANG R. Comparison between properties of polyether polytriazole elastomers and polyether polyurethane elastomers [J]. Polymers for Advanced Technologies,2014,25(3):314-321.